El proyecto NanoARPAH, desarrollado por la Universidad de Santiago de Compostela (USC) y en colaboración con el Instituto de Investigación Sanitaria de Santiago de Compostela (IDIS), propone la utilización de una novedosa tecnología de entrega de ARNm para combatir enfermedades raras como la enfermedad de Hurler.

Imágenes de microscopia electrónica de barrido (SEM) de mucopolisacáridos (MPS). (a) Fragmentos de MPS, (b) MPS de película, (c), MPS fibrosos y (d) MPS esféricos, (e) MPS fibrosos y (f) MPS de película. (a), (b) y (d) fueron recogidas en Pekín, China; (c) fue recogida en Pekín, China por Li et al. (2020), con permiso de Elsevier (Número de licencia: 5223390347409); (e) y (f) fueron recogidas en Hangzhou, China.
De acuerdo con la Organización Mundial de la Salud (OMS), se define como enfermedad rara toda aquella patología que se presenta en menos de cinco personas por cada 10 mil habitantes. Actualmente, en el mundo se han identificado casi siete mil afecciones que pueden englobarse bajo esa definición, siendo una de las más peculiares – con solo una frecuencia de 1 en cada 100.000 nacimientos – el Síndrome de Hurler.
UN TRASTORNO AUTOSÓMICO RECESIVO
Esta afección tan infrecuente se origina por la deficiencia de una enzima, la α-L-iduronidasa, cuya ausencia provoca múltiples afectaciones desde el nacimiento. Conocida también bajo las siglas MSP I, el Síndrome de Hurler causa la acumulación progresiva y excesiva de mucopolisacáridos (mucosas) en las células del tejido conectivo, así como en el hueso y en el cartílago, provocando en los pacientes que lo sufren un retraso en el desarrollo motor y mental, así como múltiples deformidades en el esqueleto y, en la mayor parte de los casos, enanismo.
El déficit protagonista de este trastorno deriva de un trastorno autosómico recesivo asociado al brazo corto del cromosoma 4: al no contar con los recursos genéticos necesarios, la enzima no se produce y las personas afectadas no disponen de la herramienta indispensable para romper las largas cadenas de moléculas de azúcar (glucosaminoglucanos). Consecuentemente, estas moléculas se acumulan en forma de mucosas, dando lugar a dificultades motrices y daños en múltiples órganos, incluyendo el corazón.

Comparación del almacenamiento lisosomal en los riñones, la membrana sinovial y la válvula mitral en una persona que padece Síndrome de Hurler (MPS I) y otra que no. Fuente: Patricia I. Dickson, MD.
LOS RETOS DEL REEMPLAZO ENZIMÁTICO
A pesar de ser una patología descubierta a principios del siglo XX, concretamente en 1919 por Gertrud Hurler, este síndrome no cuenta con un tratamiento efectivo que termine con la afección. Sin embargo, sí existen ciertos procedimientos que tienen el objetivo de mejorar las condiciones de vida de los pacientes, paliando algunos de los síntomas más incómodos y molestos. Uno de ellos es el reemplazo enzimático, una técnica que sustituye la enzima ausente o dañada por otra en perfecto estado.
No obstante, a pesar de que el reemplazo enzimático sí permite aumentar la movilidad articular por la disminución de acumulación de la molécula en las partes blancas, presenta ciertos retos significativos: la displasia ósea no mejora debido al alto peso molecular de la enzima, lo que dificulta el paso de la matriz intracelular del cartílago y el hueso. Además, cuando el tratamiento se administra de forma intravenosa, se vuelve difícil que la nueva enzima atraviese la barrera hematoencefálica, dificultado su acceso a algunos tejidos y generando una respuesta inmune demasiado fuerte y agresiva.
NANOARPAH: UNA NUEVA ESPERANZA PARA EL SÍNDROME DE HURLER
Con el objetivo de vencer esas barreras y desarrollar un tratamiento más efectivo contra esta enfermedad, nace el proyecto NanoARPAH, liderado por investigadores de la Universidad de Santiago de Compostela (USC) y en colaboración con el Instituto de Investigación Sanitaria de Santiago de Compostela (IDIS), como parte del Plan Complementario de Biotecnología Aplicada a la Salud en Galicia.
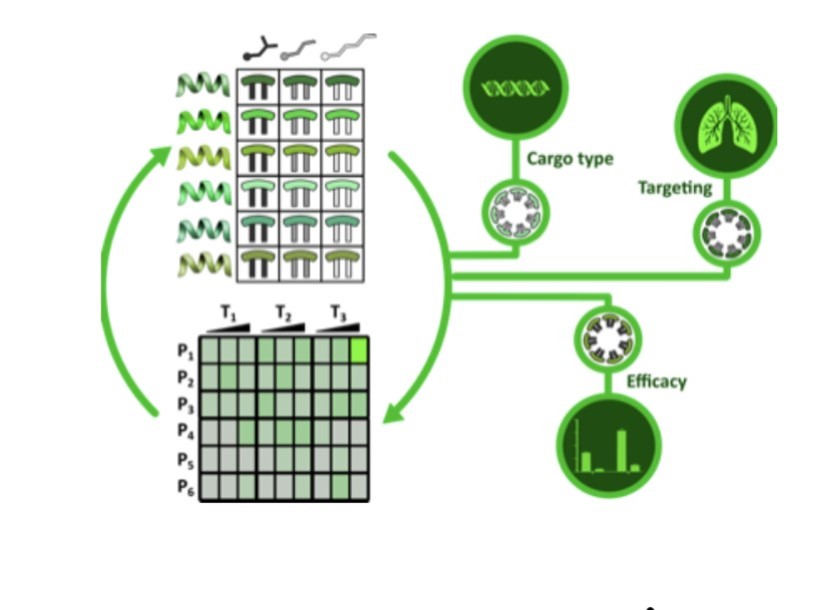
Imagen representativa del proyecto NanoARPAH
Este proyecto plantea la aplicación de una técnica novedosa de entrega de ARN mensajero (ARNm) para llevar a cabo en transporte de un ARN terapéutico que permitirá la expresión de la proteína ausente en esta enfermedad. De esta forma, el paciente podría contar con una herramienta para romper las cadenas moleculares de azúcar y evitará la acumulación de estas en los tejidos, huesos y órganos, previniendo los daños derivados de ello.
NanoARPAH se implementaría siguiendo un esquema de dos fases. En una primera, se realizaría la síntesis, caracterización y formulación de esos nanovehículos de ARNm; mientras que, en la segunda, se realizaría la evaluación preclínica del procedimiento, tanto en un formato in vitro como in vivo. En su conjunto, el éxito del proyecto supondría una auténtica revolución terapéutica para los pacientes afectados por el síndrome.