ScreenTech-ANTCANRES
Degradadores moleculares de SFN para sensibilizar células tumorales de cabeza y cuello (HNSCC) resistentes a terapias convencionales
LÍNEA DE ACTUACIÓN 3: PLATAFORMA DE CRIBADO DE FÁRMACOS Y ANÁLISIS DE INTERACCIONES FÁRMACO-DIANA
Palabras clave: Cáncer de cabeza y cuello, otros tumores sólidos; resistencia; tecnología HiBiT
Coordina: Vall d´Hebron Institut de Recerca, Barcelona (Cataluña)
Participa: Universidad de Santiago de Compostela (Galicia); Universidad del País Vasco (País Vasco)
Persona de contacto: Matilde E. Lleonart | matilde.lleonart@vhir.org
RESUMEN PROYECTO
Este proyecto se centra en una nueva terapia contra una proteína sobre-expresada en células resistentes del cáncer de cabeza y cuello (HNSCC), denominada Stratifin (SFN). Se cree que la sobre-expresión de SFN es uno de los motivos de resistencia a drogas quimioterápicas (principalmente al Cisplatino) y fallos en los tratamientos de pacientes con cáncer.
Por otro lado, existe una gran necesidad terapéutica en los pacientes con HNSCC puesto que, a pesar de que la inmunoterapia está mostrando resultados muy prometedores en pacientes metastásicos, actualmente el tratamiento en tumores HNSCC primarios no ha mostrado avances muy significativos.
Para afrontar estas dificultades, nos proponemos sensibilizar a las células cancerosas resistentes inhibiendo la función de SFN. Nuestro plan de trabajo incluye 4 objetivos principales:
1) Identificación degradadores de la proteína SFN mediante el uso de la tecnología HiBiT con detección por bioluminiscencia; partiendo de una biblioteca de múltiples compuestos/drogas.
2) Clasificación estructural, priorización de series químicas mediante estudios in vitro con líneas celulares y estudios virtuales mediante estudios de interacción con inteligencia artificial.
3) Eficacia de los compuestos priorizados en diferentes modelos celulares.
4) Ejecución de modificaciones químicas en 1-3 compuestos/drogas priorizadas para aumentar su eficacia terapéutica tanto in vitro en líneas celulares en cultivos como in vivo mediante el uso de ratones.
Con las nuevas drogas descubiertas resultantes de este proyecto, desestabilizaremos a SFN en tumores humanos que crezcan en modelos murinos como estudios pre-clínicos para idealmente proponer nuevos fármacos aplicables en pacientes HNSCC. Esta terapia también podría aplicarse a otros tumores sólidos donde SFN tiene un papel oncogénico.
RESULTADOS DEL PROYECTO
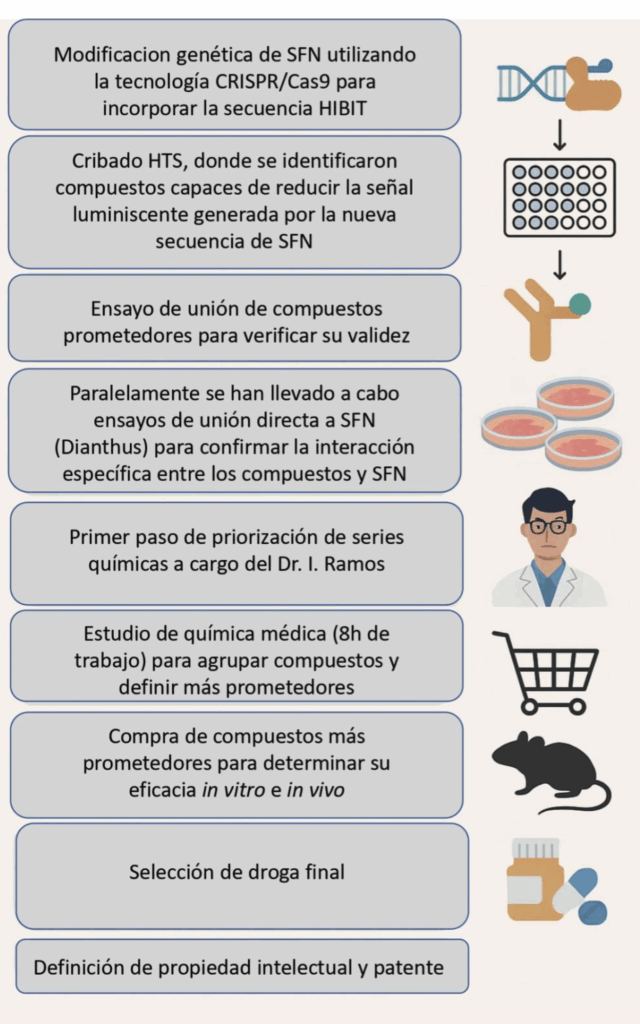
El presente proyecto ha permitido identificar pequeñas moléculas candidatas con capacidad para inducir la degradación de SFN mediante un enfoque experimental dual. En primer lugar, se modificó genéticamente el gen SFN utilizando tecnología CRISPR/Cas9 para incorporar una secuencia HiBiT, que permite cuantificar su abundancia mediante luminiscencia. A través de un cribado HTS de 102825 compuestos, se identificaron 1058 compuestos capaces de reducir dicha señal más de un 27,7%, indicando una posible degradación de SFN. Los hits positivos se reanalizaron para validar su reproducibilidad (902 compuestos confirmados en duplicado, 85% de confirmación), y se complementaron con ensayos de viabilidad celular (CellTiter-Glo) para descartar posibles falsos positivos derivados de citotoxicidad general (314 de los 902 compuestos, 34,8%, comprometen la viabilidad celular con porcentajes mayores o iguales al 30 %). En paralelo, se llevaron a cabo ensayos de unión directa a SFN (Dianthus) para confirmar la interacción específica entre los compuestos candidatos y la proteína SFN y se encontraron 80 compuestos de los confirmados (8,8%) que confirman unión al target de interés. Con los resultados de los ensayos del cribado de HTS y el ensayo de unión se ha hecho una primera clasificación de los compuestos en series químicas por la misma plataforma de screening del IRB a cargo del Dr. Israel Ramos. Actualmente, los compuestos identificados están siendo clasificados en clústeres químicos por el químico médico con el objetivo de seleccionar los más prometedores para ensayos funcionales in vitro y, posteriormente, estudios in vivo.
Este proyecto representa un enfoque pionero en la degradación dirigida de SFN como estrategia terapéutica innovadora frente al HNSCC, con el potencial de revertir la resistencia tumoral y mejorar significativamente la eficacia del tratamiento. Al centrarse en una proteína clave asociada al fallo terapéutico y al mal pronóstico, esta propuesta abre nuevas vías para el desarrollo de terapias más efectivas, no solo en HNSCC, sino también en otros tipos de cáncer donde SFN está implicada. La originalidad de la estrategia y su sólida base experimental refuerzan su alto valor traslacional y su relevancia científica
COORDINA:
PARTICIPA:


